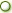ברינסוויי: אישור אירופי למכשיר החברה לטיפול באוטיזם, סכיזופרניה וגמילה מעישון
האישור מהאיחוד האירופי למכשיר ה-Deep TMS, הגיע לאחר שבתחילת השנה קיבלה החברה את אישור ה-FDA לטיפול בחולי דיכאון שטיפול תרופתי לא שיפר את מצבם
חברת בריינסווי, העוסקת במחקר ופיתוח של מכשיר רפואי לטיפול בהפרעות בתפקודי המוח, מדווחת היום כי קיבלה את אישור ה-CE Marketing של האיחוד האירופי לשיווק המוצר Deep TMS באירופה לטיפול באוטיזם, לטיפול בחולי אלצהיימר ולגמילה מעישון. האישור הוענק על ידי MedCert, הגוף המוסמך להעניק את האישורי מטעם ה-CE Marketing.
- בריינסווי הפסידה 22 מיליון שקל ב-2012; עלות שכר המנכ"ל - 1.8 מיליון שקל
- בריינסוויי: טיפול במכשיר החברה בתדירות גבוהה יעיל בגמילה מעישון
- בריינסווי: "הרבעון נחתום על הסכם הפצה בארה"ב ולאחריו נצא להנפקה בנאסד"ק"
ארגון CE Marketing הוא הגוף האחראי מטעם מדינות האיחוד האירופי על מתן אישור לשיווק מוצרים במדינות הגוש האירופי. כל מוצר המשווק באירופה נדרש לאישור הארגון, שמבצע למוצר בדיקות בטיחות, בריאות ואיכות סביבה סביבה.
 בריינסווי
בריינסווי
בריינסווי מוסיפה בדיווח כי היא קיבלה אישור להתחלת שיווק מיידי של מכשיר ה-Deep TMS להתוויות טיפוליות נוספות לאחר והשלמת הניסויים הקליניים וועדכון התיק הטכני למכשיר - מבלי להידרש לבקשת אישור מיוחדת.
בתחילת השנה קיבלה בריינסווי בניהולו של עוזי סופר, אישור מנהל המזון והתרופות בארה"ב (FDA) לטיפול במכשיר ה-Deep-TMS של החברה בחולי דיכאון, שטיפול תרופתי לא הביא לשיפור במצבם. הכנסות בריינסווי ממכירת המכשירים שפיתחה הסתכמו ב-2012 ב-1.36 מיליון שקל, לעומת הכנסות של 979 אלף שקל ב-2011.
| קנייה חזקה | קנייה | המתן | מכירה | מכירה חזקה |
לפני כשבוע דיווחה בריינסוויי כי גייסה 6.3 מיליון דולר מקבוצת משקיעים פרטיים לפי מחיר של 60 שקל למניה - מחיר הנמוך ממחיר הבסיס של המניה בבורסה ב-8%.